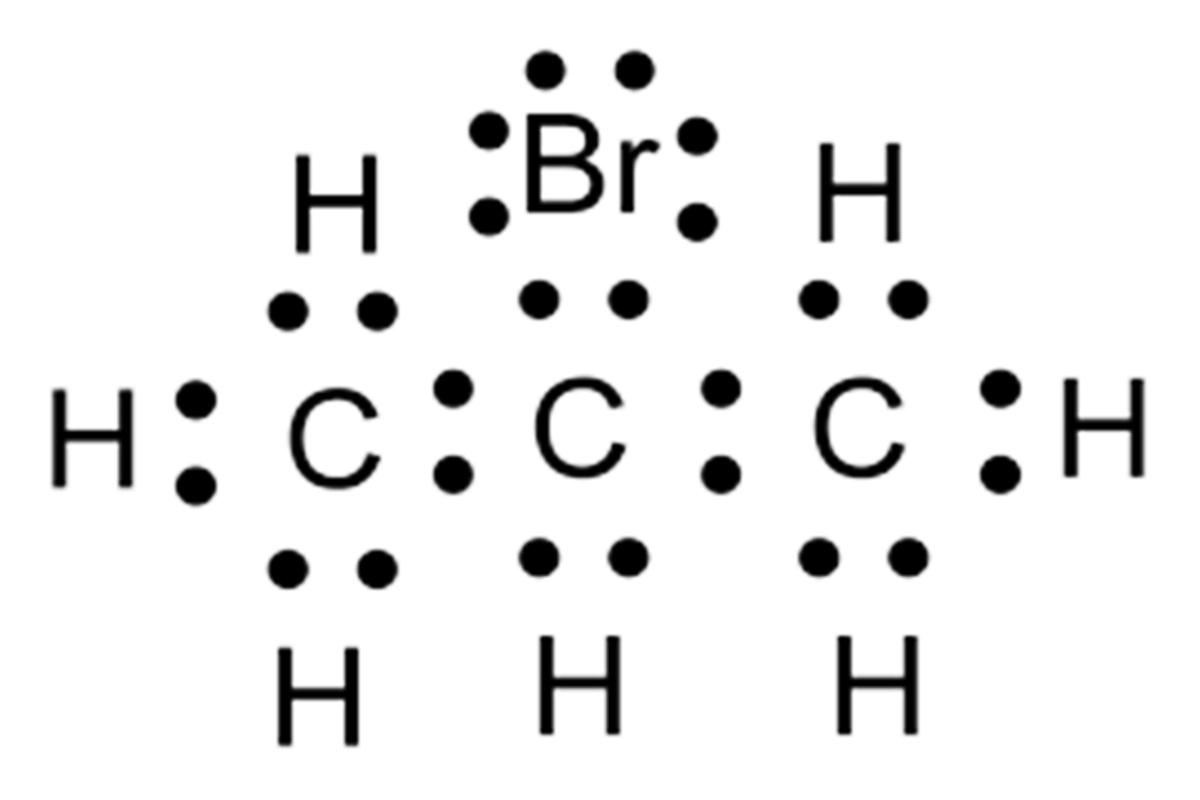
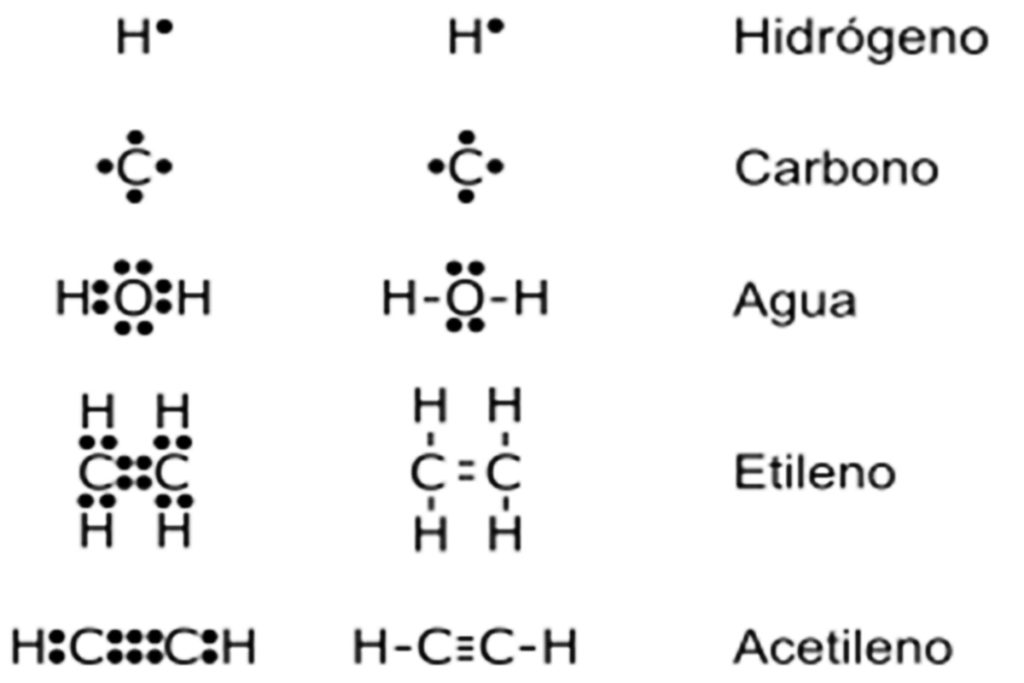
Cuando las personas hablan de átomos o moléculas, siempre está de por medio la estructura de Lewis. Pero, son muy pocas las personas que realmente saben todo acerca de la misma, debido a que parece ser bastante compleja.
Por ello, a continuación te traemos un post muy completo donde podrás informarte al máximo acerca de la estructura de Lewis. Te aseguramos que podrás resolver todas tus dudas, simplemente… ¡Lee hasta el final!
¿Qué es la estructura de Lewis?
Básicamente, la estructura de Lewis es una representación sencilla de la formación de átomos o moléculas que se hacen dentro de un ion. Se suele representar en puntos largos y por ende, puede servirnos para saber la reacción del mecanismo.
¿Cómo puedo realizar una estructura de Lewis?
Realmente, realizar una estructura de Lewis es bastante sencillo. Simplemente, debes saber la formula química de cada compuesto. Partiendo de allí, solo ubicas cada uno en su respectivo grupo. Aunque, para los metales de transición, esto suele ser un poco diferente. Pero…
¿Cuál es la fórmula química de la estructura de Lewis?
Aquí es donde las personas se enredan mucho, debido a que, se ponen a crear diversas fórmulas erróneas para poder crearla. Por ello, a continuación te la mostraremos y, aunque no lo creas, es bastante sencilla. Esta es:
C = N – D.
Significado:
C: La letra “C” significa el número de los enlaces que deben elaborarse o crearse, debido a que son los electrones compartidos. Por ende, si vez un número junto a dicha letra, ya sabes lo que tienes que hacer.
N: La letra “N” es la más relevante de la formula, debido a que, son los electrones que más se necesitan en ella.
D: La letra “D” es la más simple de todas, ya que, ella solo relaciona los electrones que están disponibles para formar la estructura.
Ejemplos de la estructura de Lewis
Para que entiendas como se debe elaborar o realizar una estructura de Lewis de manera sencilla, a continuación te mostraremos unos ejemplos que te servirán de mucha ayuda. Estos son:
EJEMPLO 1 – El amoníaco
El amoníaco es uno de los más solicitados cuando de estructura de Lewis se trata. Por ello, decidimos incluirlo en nuestros ejemplos. Según la formula, el amoniaco podría quedar de la siguiente manera:
D: En los electrones disponibles encontrarás “1×5” y un “1×3”, debido a que, habrá 5 átomos de nitrógeno y tres de hidrogeno. Lo cual, daría un total de 8 electrones.
N: La letra “N” vendría quedando con un “8×1” más un “2×3”. Para un total de 14 electrones.
C: Debido a las dos letras anteriores, los electrones que deben quedarse son 6, ya que eso es lo que da la resta de 14-8.
Por ende, todo se resumiría en un “C/2=3 enlaces de estructura de Lewis”.
EJEMPLO 2 – El yodo
Si no entendiste el ejemplo uno, te mostraremos uno más fácil: el yodo. El mismo es sumamente sencillo de explicar mediante estructura de Lewis porque solo vendría siendo la siguiente formula:
D: En los electrones disponibles encontrarás un “2×7” para un total de 14 electrones.
N: Los electrones necesarios vendrían siendo 16, debido a sus números: “2×8”.
C= Debido a lo anterior, los enlaces que se deben crear son 2, debido a que es el resultado de 16-14.
Por ende, todo se resumiría en un “C/2= 1 enlace de estructura de Lewis”.
Finalmente, esperamos que con este post hayas entendido todo lo que debes saber acerca de la estructura de Lewis. ¿Qué piensas tú sobre ella?